Незважаючи на понад 35 років досліджень, вчені досі не знайшли ліки від вірусу імунодефіциту людини (ВІЛ): вірусу, який викликає синдром набутого імунодефіциту (СНІД).
Антиретровірусна терапія (АРТ) стала головним проривом, який допомагає придушити вірус, але це не ліки. І хоча було кілька широко розрекламованих випадків, коли, як говорили, ВІЛ-інфекція була вилікувана - у тому числі Тімоті Брауна, він же Берлінський пацієнт, - досі не існує підходу, який може послідовно та безпечно викорінювати ВІЛ на індивідуальній основі , а тим більше у світовому масштабі. Незважаючи на це, прогрес досягається.
ТЕК ЗОБРАЖЕННЯ / НАУКОВА ФОТОБІБЛІОТЕКА / Getty Images
Виклики
Існує декілька причин, чому пошук ліків від ВІЛ / СНІДу був таким довгим шляхом для кожного. ВІЛ - настільки складний, багатогранний вірус, що постійно змінюється, що ускладнює його встигання.
Деякі із сучасних загальних проблем, з якими стикаються дослідження щодо ВІЛ, включають:
- Охоплення груп населення, найбільш ризикованих зараженням та передачею ВІЛ
- Забезпечення того, щоб дослідження проводилось за поінформованою згодою учасників, тобто вони повністю розуміли як ризики, так і переваги випробування
- Розробка безпечних та ефективних кандидатів на вакцину проти ВІЛ для тестування за допомогою клінічних випробувань як з приматами, так і з людьми
- Поглиблення розуміння механізмів імунної відповіді у людей
- Враховуючи в дослідженнях супутні захворювання на ВІЛ, будь-яке потенційне лікування виграє якомога більшій кількості людей
- Збільшення уваги до вивчення ремісії спостерігається у рідкісних пацієнтів, які припинили лікування
- Визначення того, що саме означає «ліки» від ВІЛ
- Зменшення стигми, яка все ще оточує ВІЛ, з метою мінімізації її впливу на участь у дослідженнях щодо ВІЛ
- Поглиблення розуміння того, як ефективно лікувати коінфекції ВІЛ та керувати невдалими в лікуванні
Зниження передачі
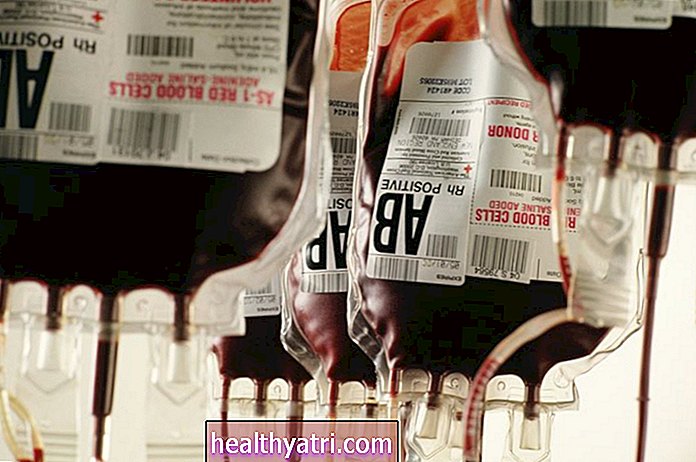
Хоча це не є "лікуванням", як таке, стратегія "лікування як профілактика" (TasP), що включає щоденний прийом ліків від ВІЛ, має високу ефективність у зменшенні передачі інфекції для тих, хто вже є ВІЛ-позитивним.
Більше того, у 2020 році було оголошено, що тривалість життя хворих на ВІЛ у Сполучених Штатах така ж, як і тих, хто ніколи не інфікувався вірусом, хоча вони мали набагато менше років міцного здоров'я.
В ідеалі наступним кроком буде розробка безпечної та ефективної вакцини проти ВІЛ, але в даний час існують певні труднощі, що перешкоджають прогресу, який досягається в ході дослідження.
Генетична мінливість
Однією з найважливіших перешкод для створення широко ефективної вакцини проти ВІЛ є генетичне різноманіття та мінливість самого вірусу.
Виклик циклу реплікації
Замість можливості зосередитись на одному штамі ВІЛ, дослідникам доводиться враховувати той факт, що він так швидко розмножується, що може спричинити мутації та нові штами. Цикл реплікації ВІЛ займає трохи більше 24 годин.
І хоча процес реплікації швидкий, він не найточніший - щоразу створюється багато мутованих копій, які потім об’єднуються, утворюючи нові штами, коли вірус передається між різними людьми.
Наприклад, у ВІЛ-1 (окремий штам ВІЛ) існує 13 різних підтипів та підтипів, які пов’язані географічно, з різницею від 15 до 20% у межах підтипів та варіацією до 35% між підтипами.
Це не лише проблема у створенні вакцини, але й тому, що деякі мутовані штами стійкі до АРТ, а це означає, що деякі люди мають більш агресивні мутації вірусу.
Латентні водойми
На додаток до постійно розвиваються та мутуючих штамів ВІЛ, ще однією проблемою у розробці вакцини є щось, що називається латентними резервуарами. Вони встановлюються на самій ранній стадії ВІЛ-інфекції та можуть ефективно «приховати» вірус від імунного виявлення, а також наслідків АРТ.
Це означає, що якщо лікування буде коли-небудь припинено, латентно інфікована клітина може бути реактивована, що призведе до того, що клітина знову почне виробляти ВІЛ.
Хоча АРТ може придушити рівень ВІЛ, він не може ліквідувати приховані резерви ВІЛ - це означає, що АРТ не може вилікувати ВІЛ-інфекцію.
Виснаження імунітету
Існує також проблема виснаження імунітету, яке виникає при тривалій ВІЛ-інфекції. Це поступова втрата здатності імунної системи розпізнавати вірус та запускати відповідну відповідь.
Будь-який тип вакцини проти ВІЛ, лікування СНІДу чи іншого лікування повинен створюватися з урахуванням виснаження імунітету, пошуку шляхів вирішення та компенсації зменшення можливостей імунної системи людини з часом.
Ранній прогрес
Незважаючи на те, що прогрес, досягнутий у лікуванні ВІЛ-інфекції, повільний, все ще залишаються проблиски надії, що вказує на те, що вчені можуть наближатись до широко ефективного лікування.
Берлінський пацієнт
Мабуть, найбільш відомим випадком на сьогоднішній день був Тімоті Браун, також відомий як "Берлінський пацієнт", який вважається першою людиною, яка "функціонально вилікувалася" від ВІЛ.
Незважаючи на своє прізвисько, Браун народився в США, але в 1995 році під час навчання в Німеччині йому поставили діагноз ВІЛ. Через десять років у нього діагностували гострий мієлоїдний лейкоз (ОМЛ) і йому потрібна була трансплантація стовбурових клітин, щоб мати шанс пережити рак.
Коли лікарі виявили, що Браун співпадає з 267 донорами (багато людей не знаходять жодного збігу), вони вирішили використати того, хто мав мутацію під назвою CCR5-delta 32, яка, як вважалося, могла викликати імунітет до ВІЛ.
Через три місяці після трансплантації в лютому 2007 року ВІЛ більше не виявлявся в крові Брауна. І хоча він продовжував мати ускладнення з лейкемією - і вимагав додаткової трансплантації стовбурових клітин - ВІЛ-інфекція Брауна не повернулася. Так залишалося до його смерті в 2020 році від лейкемії.
Лікарі Бригамської та Жіночої лікарні в Бостоні намагалися застосувати подібну техніку трансплантації стовбурових клітин у двох пацієнтів у період з 2008 по 2012 рік, хоча і не використовуючи донорів з мутацією дельта 32. Незважаючи на те, що спочатку пацієнти пережили 10 і 13 місяців невизначеного рівня ВІЛ, вони обидва згодом пройшли вірусний рикошет.
Лондонський пацієнт
Було опубліковано дослідження 2019 року, що містить деталі стосовно другої людини - Адама Кастіллехо, цього разу відомого як "лондонський пацієнт", який також, здається, функціонально вилікувався від ВІЛ.
Його ситуація була подібна до ситуації Брауна, оскільки він страждав на рак, отримував хіміотерапію, щоб знищити свою імунну систему, а потім пересадив стовбурові клітини з використанням донорських клітин з генетичною мутацією, що призводить до імунітету до ВІЛ.
Наразі є клінічні докази того, що Кастіллехо перебуває у стадії ремісії ВІЛ-1 протягом 30 місяців, не виявляючи вірусу, компетентного до реплікації, хоча незрозуміло, чи буде це продовжуватися.
І хоча використання трансплантації стовбурових клітин для вироблення імунітету проти ВІЛ, можливо, було успішним для Брауна та Кастильєхо, це не те, що буде використано в теперішній формі у звичайній клінічній практиці найближчим часом.
Цей багатоступеневий процес не тільки дорогий, але й включає занадто багато потенційних ризиків та шкоди для пацієнта.
Оскільки Браун і Кастіллехо мали рак і все одно потребували трансплантації стовбурових клітин, пошук донора з мутацією дельта 32 мав сенс. Однак для тих, хто не страждає на рак, неможливо пройти цей специфічний курс лікування.
Незважаючи на практичні обмеження лікування, ці випадки запропонували вченим уявлення, які суттєво вдосконалили дослідження лікування ВІЛ.
Генна терапія на основі стовбурових клітин
Одним із видів лікування, який демонструє початковий потенціал, є генна терапія на основі стовбурових клітин - підхід, значною мірою відомий у випадку Брауна.
Його метою є відновлення імунної системи ВІЛ шляхом трансплантації генетично сконструйованих гемопоетичних стовбурових клітин генами проти ВІЛ, які можуть не тільки самовідновлюватися, але й розмножуватися та диференціюватися у зрілі імунні клітини.
Досягнуто певного успіху в ранніх дослідженнях генної терапії на основі стовбурових клітин.
Дослідження 2018 року за участю мавп-макак, інфікованих ВІЛ-інфекцією, виявило, що трансплантація відредагованих генами стовбурових клітин змогла значно зменшити розмір їх сплячих "вірусних резервуарів", які могли реактивуватися для отримання додаткових копій вірусу.
З тих пір був досягнутий додатковий прогрес з приматами. Згідно з дослідженням 2021 року, дослідники визначили формулу, яка передбачала б ідеальну дозу стовбурових клітин, необхідну для лікування ВІЛ.
Ще слід виконати роботу
Незважаючи на те, що підхід продемонстрував обіцянку у приматів, він у жодному разі не можна відтворити у глобальному масштабі.
Зараз мета полягає у відтворенні наслідків трансплантації стовбурових клітин Брауна та Кастільйо в інших людей, але без токсичності необхідності проходити хіміотерапію спочатку.
Широко нейтралізуючі антитіла
Деякі з найперспективніших моделей вакцин на сьогодні включають широко нейтралізуючі антитіла (bNAbs) - рідкісний тип антитіл, здатний орієнтуватися на більшість варіантів ВІЛ.
BNAbs вперше були виявлені у кількох контролерів еліти ВІЛ - людей, які, здається, мають здатність придушувати реплікацію вірусів без АРТ і не свідчать про прогресування захворювання. Деякі з цих спеціалізованих антитіл, такі як VRC01, здатні нейтралізувати понад 95% варіантів ВІЛ.
В даний час дослідники вакцин намагаються стимулювати вироблення bNAbs.
Дослідження 2019 року, в якому беруть участь мавпи, показує перспективу. Отримавши один постріл вакцини проти ВІЛ, шість із 12 мавп, які брали участь у дослідженні, виробили антитіла, які значно затримували зараження, і, у двох випадках, навіть запобігали цьому.
bNAbs, що показують обіцянку
Цей підхід все ще знаходиться на ранніх стадіях випробувань на людях, хоча в березні 2020 року було оголошено, що вперше вчені змогли розробити вакцину, яка спонукала клітини людини до генерування bNAbs.
Це є помітним розвитком за роки минулих досліджень, які до цього моменту були стримувані відсутністю надійної або специфічної реакції bNAb.
Зміна латентності
Поки вчені не зможуть «очистити» приховані резервуари ВІЛ, навряд чи будь-яка вакцина або терапевтичний підхід повністю знищить вірус.
Деякі агенти, включаючи інгібітори HDAC, що використовуються в терапії раку, показали перспективність, але досі не змогли досягти високого рівня кліренсу без ризику токсичності. На додачу до цього, вчені досі не впевнені, наскільки великими є ці водосховища.
Однак сподіваємося, що поєднання агента, що зменшує затримки, з вакциною (або іншими стерилізуючими агентами) може досягти успіху за допомогою лікувальної експериментальної стратегії, відомої як "удар і вбивство" (вона ж "удар і вбивство") що зараз розслідується.
Стратегія ногами
Це двоступеневий процес:
- По-перше, препарати, які називаються агентами, що зворотять латентність, використовуються для реактивації прихованого ВІЛ, що ховається в імунних клітинах (частина "удару" або "удару").
- Потім, як тільки імунні клітини реактивуються, імунна система організму - або препарати проти ВІЛ - можуть націлювати та вбивати реактивовані клітини.
На жаль, лише агенти, що зменшують затримки, не здатні зменшити розмір вірусних водойм.
Інша стратегія скасування латентності може включати інгібітори PD-1, такі як Кейтруда (пембролізумаб), які показали перспективність при очищенні вірусних резервуарів, одночасно потенційно зменшуючи виснаження імунітету.
PD-1 діє як імунна контрольна точка і переважно експресується на поверхні постійно інфікованих клітин. Але на даний момент досі незрозуміло, чи PD-1 відіграє функціональну роль у затримці ВІЛ та стійкості резервуару.
Слово з дуже добре
Поки досягається прогрес у досягненні ліків від ВІЛ, ще рано говорити, коли може відбутися прорив.
На щастя, вчені досягли значних успіхів у профілактиці ВІЛ - особливо завдяки попередній експозиційній профілактиці (або PrEP). Ідея PrEP полягає в тому, щоб дати людям із високим ризиком зараження ВІЛ, але не інфікованими, можливість запобігти цьому, приймаючи таблетки один раз на день. При правильному та послідовному використанні PrEP знижує ризик зараження ВІЛ від статевих стосунків приблизно на 99%, а від ін’єкційних наркотиків - на 74%.
Але поки не буде знайдено ліки, найкращим результатом для людей з ВІЛ є антиретровірусна терапія, яка може зменшити ризик ВІЛ-асоційованих захворювань і зберегти тривалість життя для тих, хто живе в США, на таку ж тривалість, як і тих, хто цього не робить. мають ВІЛ.
.jpg)