AaronP / Bauer-Griffin / Contributor / Getty Images
Ключові винос
- Одноразова вакцина проти коронавірусу Джонсона та Джонсона викликала імунну відповідь проти COVID-19 у клінічних випробуваннях.
- Клінічні випробування говорять про те, що вакцина на 66% ефективно запобігає помірному та тяжкому перебігу захворювання через 28 днів після вакцинації та 72% ефективна в США
- Одноразова вакцина була б корисною для поточного процесу вакцинації в США, який в даний час вимагає логістичного планування вакцин, які потребують двох доз.
- Якщо вакцина компанії дозволена Управлінням з контролю за продуктами та ліками США (FDA), це буде третя вакцина, дозволена для використання в США.
Останні результати клінічного випробування фази 3 показують, що одноразова вакцина проти коронавірусу від Джонсона та Джонсона на 66% ефективна проти помірного та важкого COVID-19.
Результати відображають ефективність вакцини у всьому світі, а рівень захисту різний у всьому світі. Хоча вакцина була ефективною на 72% серед учасників США, вона була ефективною лише на 57% серед учасників у Південній Африці, де вперше з’явився варіант високотрансмісивного SARS-CoV-2.
Примітно, що нікому в клінічному дослідженні не потрібно було госпіталізувати COVID-19, і ніхто не помер від цієї хвороби.
Хоча загальна ефективність нижча, ніж 95%, продемонстрована як Moderna, так і Pfizer, вакцина Johnson & Johnson приносить із собою два перспективні фактори, яких не мають дводозові вакцини Moderna та Pfizer: перший полягає в тому, що заклади охорони здоров'я будуть стикатися з меншою логістикою планування при введенні однодозової проти дводозової вакцини. Вакцину також можна тримати в холодильнику протягом трьох місяців, на відміну від вакцин Moderna та Pfizer, які повинні зберігатися в морозильній камері до використання, що робить збереження складним для деяких закладів охорони здоров’я.
Раніше цього місяця результати клінічних випробувань фази 1 / 2а показали, що вакцина компанії викликала імунні реакції проти SARS-CoV-2, вірусу, що викликає COVID-19, як серед молодих, так і серед літніх учасників.
Згідно з доповіддю, Johnson & Johnson випадковим чином призначили здоровим дорослим людям у віці від 18 до 55 років та людям від 65 років отримувати або високу, або низьку дозу вакцини, або плацебо. Обрана група учасників когорти з 18 до 55 отримала другу дозу вакцини. Загалом у суді брали участь 805 учасників.
"Більшість добровольців виробляють виявляються нейтралізуючі антитіла, які, на думку дослідників, відіграють важливу роль у захисті клітин від вірусу, згідно з даними випробувань", - йдеться у заяві Johnson & Johnson. у всіх добровольців були виявлені антитіла, незалежно від дози вакцини або вікової групи, і вони залишались стабільними принаймні 71 день у віковій групі від 18 до 55 років ».
Компанія співпрацює зі своїм фармацевтичним відділом Янссен над розробкою вакцини.
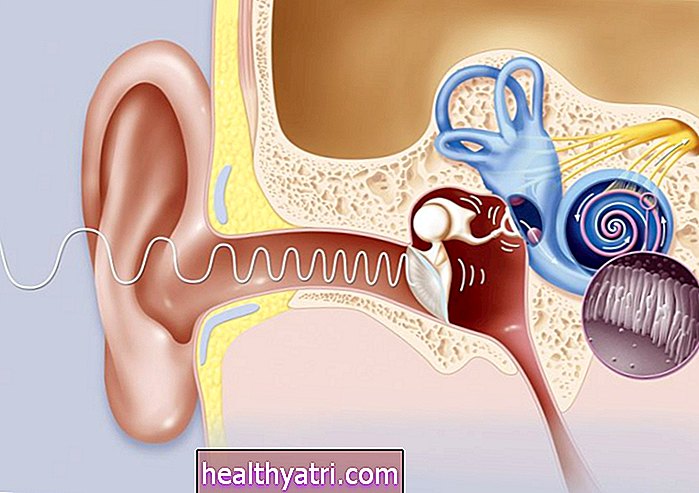
Що таке імунна відповідь?
Вироблення імунної відповіді є необхідним етапом у процесі створення вакцин. Простіше кажучи, при зараженні новим вірусом імунна система реагуватиме на це, використовуючи ряд засобів для боротьби з мікробами, необхідних для подолання інфекції, повідомляє Центр контролю та профілактики захворювань (CDC). якщо інфекція очиститься, імунна система «згадає» те, що вона дізналася про те, як захистити організм від цієї хвороби, і застосує це проти будь-яких майбутніх інфекцій.
"Ваша імунна система захищає вас від хвороб", - говорить Сома Мандал, доктор медичних наук, спеціаліст, що пройшов сертифікацію в Нью-Джерсі. "Коли імунна система (що складається з різних органів) визнає певний зародок (наприклад, бактерії, віруси) чужорідним, вона запускає антитіла, які допомагають знищити зародок".
Мандал каже, що цей процес називають імунітетом В-клітин. Імунітет до Т-клітин, навпаки, виникає, коли "імунна система запам'ятовує певний мікроб і знищує його, перш ніж він знову може захворіти".
Вакцини діють подібним чином, за винятком того, що вони створені для імітації інфекції, тобто імунна система запам'ятовує і захищає, не заходячи людині, щоб зробити це, каже Мандал. Звичайно, незначні симптоми можуть виникати в результаті вакцинації.
Johnson & Johnson’s Early Results
У жовтні Johnson & Johnson оголосили ранні результати, які показують, що одна доза їх вакцини може викликати антитіла у 97% учасників дослідження, які ефективно нейтралізують вірус у лабораторії, але компанія все ще вимагала додаткової інформації про ефективність вакцини. U
Потім вони зазнали невдач у своїх випробуваннях, коли учасник пережив незрозумілу хворобу. Конкретних деталей щодо того, що сталося через конфіденційність пацієнта, не було надано. Регулятори визначили, що 23 жовтня подія не була пов'язана з вакциною, і випробування було безпечно відновити.
Оцінка безпеки
Учасники всіх трьох груп (високі дози, низькі дози та плацебо) клінічних випробувань повідомили про слабкі симптоми, включаючи:
- Головний біль
- Втома
- Нудота
- Міалгія (біль у м'язах)
- Біль у місці ін’єкції
Побічні реакції були менш поширеними у старшій віковій групі. У випадку учасників, які отримували схему прийому двох доз, після другої дози спостерігалося менше реакцій.
П'ятеро учасників відчули більш серйозні симптоми: один учасник відвідав лікарню з приводу лихоманки, пов'язаної з вакцинацією - учасник видужав протягом 12 годин. Решта чотири випадки були підтверджені не пов'язаними з вакциною.
Наступні кроки
Головний науковий керівник компанії Пол Стоффелз, доктор медичних наук, заявив в інтерв'ю 12 січня, що компанія Johnson & Johnson має на меті поставити мільярд доз вакцини до кінця цього року. Стоффелз заявив, що поки компанія не отримає дозвіл на екстрене використання (EUA) від Управління з контролю за продуктами та ліками США (FDA), поки ще рано говорити конкретно, скільки доз буде доступно в березні. Перш ніж рухатись вперед з EUA, FDA вимагає подальшого спостереження щонайменше за два місяці даних про безпеку половини учасників дослідження, поріг якого Джонсон і Джонсон переступили на початку цього місяця.
"Якщо однодозова вакцина виявиться безпечною та ефективною, компанія розраховує незабаром подати заявку на отримання дозволу на екстрене використання до Американської адміністрації з харчових продуктів і медикаментів, а інші регуляторні заявки у всьому світі будуть подані згодом", - заявив Джонсон Та Джонсон у своєму випуску новин.
"Ми прагнемо отримати 1 мільярд доз у 2021 році", - сказав Стоффельс. “Якщо це одна доза, це означає 1 мільярд людей. Але це буде збільшуватися протягом року ... Це кілька тижнів зарано, щоб давати остаточні цифри того, що ми можемо запустити протягом перших кількох місяців ".