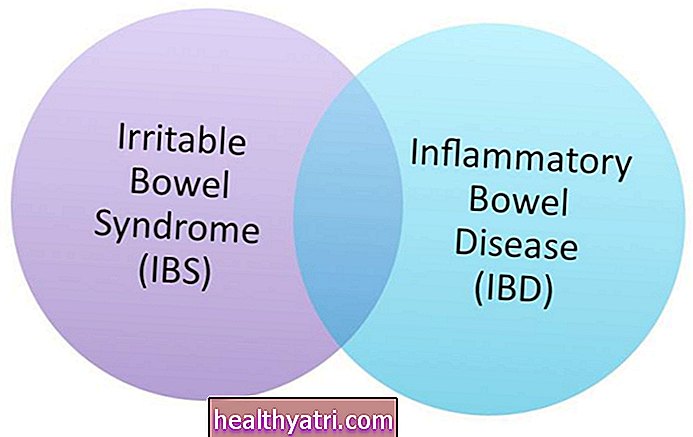
Підтипи гострого мієлоїдного (або мієлогенного) лейкозу (ОМЛ) стають все більш зрозумілими, вивчаються нові шляхи досліджень. AML сильно варіюється від однієї людини до іншої, і прогноз часто поганий. Це робить дослідження, яке може допомогти покращити рівень виживання, вирішальним.
Нові досягнення за останні кілька років покращили діагностику, лікування та показники виживання, що все надає перспективу з більшою надією.
ОМЛ - це рак крові та кісткового мозку (губчаста внутрішня частина кісток, де утворюються клітини крові). Це "гостро", оскільки швидко прогресує. "Мієлоїд" означає, що він включає мієлоїдні клітини, які розвиваються в різні типи клітин крові (наприклад, червоні та білі кров'яні клітини, тромбоцити).
Альбіна Гаврилович / Getty Images
Симптоми ПВК включають:
- Лихоманка
- Біль у кістках
- Млявість і втома
- Часті інфекції
- Легкі синці
- Незвична кровотеча
Підтипи проти постановки
Коли діагностується більшість ракових захворювань, їх «інсценують». Етап повідомляє вам, наскільки розвинений рак, визначає ваш прогноз і може керувати рішеннями щодо лікування.
AML не проводиться. Натомість ваш світогляд та лікування залежать від вашого підтипу, який визначається лабораторними тестами.
Більшість підтипів AML частково визначаються тим, як розвинені та аномальні ракові клітини виглядають під мікроскопом під час першого діагностування захворювання. Крім того, класифікація AML тепер доповнюється новими відкриттями про генетичні зміни або мутації, які беруть участь.
В даний час використовуються дві системи класифікації ПВК:
- Французько-американсько-британська (FAB) класифікація
- Класифікація Всесвітньої організації охорони здоров’я (ВООЗ)
Подальша класифікація за складними генетичними підтипами розвивається завдяки новаторському дослідженню, опублікованому в 2016 році.
Чому підтип має значення
Знання генетичного складу вашого лейкозу може допомогти вашому лікареві передбачити, чи будуть ефективні сучасні методи лікування. Це вже зробило більш масштабне генетичне тестування на момент встановлення діагнозу.
Розуміння підтипів може також допомогти дослідникам розробити нові клінічні випробування, щоб розробити найкращі методи лікування для кожного типу АМЛ.
Класифікація підтипів AML
Система класифікації FAB існує з 1970-х років, але за останні роки процес підтипу змінився кілька разів. Система класифікації ВООЗ стала стандартною в 2008 році, групуючи людей на основі генетичних змін, що лежать в основі їх раку (так звані "мутації драйверів").
Потім, у 2016 році, вМедичний журнал Нової Англії (NEJM)що зробило підтипування ще далі.
Це дослідження продемонструвало, що молекулярні класифікації ВООЗ не працюють майже для половини випадків ЛМП - 48% учасників дослідження не можуть бути класифіковані на основі молекулярних груп ВООЗ, хоча 96% з них мають мутації драйверів.
Зараз слідчі з самого початку розпочали переоцінку геномної класифікації ПВК на основі:
- Відкриття багатьох нових генів лейкемії
- Виявлення множинних мутацій водія на пацієнта
- Складні моделі мутації
Класифікація FAB по боротьбі з відмиванням коштів
Більше 40 років тому група французьких, американських та британських експертів з лейкемії поділила AML на підтипи M0 - M7 на основі типу клітини, з якої розвивається лейкемія, і того, наскільки зрілі клітини.
- Від M0 до M5 все починається з незрілих форм лейкоцитів.
- М6 починається з дуже незрілих форм еритроцитів.
- М7 починається в незрілих формах клітин, які утворюють тромбоцити.
Класифікація ВООЗ ПВК
Система класифікації FAB все ще використовується для групування AML за підтипами; однак знання просунулись стосовно факторів, що впливають на прогноз та прогноз для різних типів ПВК.
Деякі з цих досягнень знайшли своє відображення у системі Всесвітньої організації охорони здоров’я (ВООЗ) 2008 року, яка розділяє ПВК на кілька груп:
- ОМЛ із змінами, пов’язаними з мієлодисплазією
- AML, пов’язаний з попередньою хіміотерапією або опроміненням
- Мієлоїдна саркома (також відома як гранулоцитарна саркома або хлорома)
- Проліферація мієлоїдів, пов’язана із синдромом Дауна
- AML з хромосомними транслокаціями та інверсіями
- AML не вказано інакше
- Недиференційований та біфенотиповий гострий лейкоз
Групи 5, 6 та 7 далі розбиті.
AML з хромосомними транслокаціями та інверсіями
При хромосомних транслокаціях частина генетичного матеріалу відривається від свого початкового місця розташування і знову приєднується до іншої хромосоми. При інверсіях сегмент виходить, перевертається догори дном і знову приєднується до своєї початкової хромосоми.
Принаймні сім типів AML включають транслокації, інверсії або подібні генетичні аномалії.
AML не вказано інакше
Випадки ПВК, які не потрапляють до однієї з вищезазначених груп, класифікуються подібно до системи FAB.
Недиференційований та біфенотипічний гострий лейкоз
Це лейкемії, які мають як лімфоцитарну, так і мієлоїдну ознаки. Їх іноді називають:
- Гострий лімфолейкоз (ALL) з мієлоїдними маркерами
- AML з лімфоїдними маркерами
- Змішані гострі лейкози
Нові класифікації: Дослідження NEJM
Дослідження 2016 року, яке спричинило нещодавні зміни, включало 1540 людей з ПВК. Дослідники проаналізували 111 генів, які, як відомо, викликають лейкемію, з метою виявлення "генетичних тем", що лежать в основі розвитку хвороби.
Вони виявили, що учасників можна розділити щонайменше на 11 основних груп, кожна з різними кластерами генетичних змін та з різними характеристиками та особливостями захворювання.
Згідно з дослідженням, у більшості людей відбулася унікальна комбінація генетичних змін, що зумовлюють їх лейкемію, що може допомогти пояснити, чому рівень виживання при АМЛ дуже різниться. Таким чином, дослідники працювали над розробкою нової системи класифікації ПВК з використанням цієї нової інформації.
Вони дійшли висновку, що існують три підгрупи, які не враховувались у системі класифікації ВООЗ. Вони називаються:
- Хроматин-сплайсосома
- TP53-анеуплоїдія
- IDH2R172
Використовуючи запропоновану систему для класифікації 1540 учасників дослідження:
- Кожного з 1236 людей з мутаціями водіїв можна класифікувати в одну підгрупу
- 56 пацієнтів відповідали критеріям для двох або більше підгруп
- 166 людей з мутаціями водіїв залишились не класифікованими
Автори рекомендували, щоб у короткостроковій перспективі п’ять специфічних генетичних типів (звані TP53, SRSF2, ASXL1, DNMT3A та IDH2) повинні бути включені до прогностичних настанов, оскільки вони є загальними та сильно впливають на результати.
Прогностичне проти діагностичне
Дослідники NEJM закликали до двох окремих систем класифікації:
- Один для використання при діагностиці людей
- Один для використання при прогнозуванні результатів (прогноз)
Вони говорять, що діагностична система повинна базуватися на фіксованих властивостях, тоді як прогностична система повинна регулярно змінюватися на основі доступних методів лікування.
Новіші дослідження
Базуючись переважно на дослідженні NEJM, інші дослідники досліджували певні генетичні профілі AML. Згідно з дослідженнями, опублікованими в 2020 році, деякі дослідники визначили:
- Потенційні нові методи ранньої діагностики для певних підтипів
- Потенційні нові способи виявлення людей, які можуть бути резистентними до наркотиків
- Потенційні нові комбінації методів лікування резистентних до наркотиків випадків
В одному з досліджень було виявлено новий препарат, який, на думку дослідників, ефективний проти лікарських стійких підтипів AML, і після його використання "матиме негайний клінічний вплив".
Діагностування підтипів AML
Лікарі мають багато інструментів для діагностики ПВК та визначення вашого підтипу. Діагностика починається з фізичного огляду. Під час вашого іспиту вони шукатимуть такі ознаки, як:
- Широкі синці
- Кровотеча
- Інфекція
- Аномалії в очах, роті, печінці, селезінці або лімфатичних вузлах
Для підтвердження підозри на діагноз ЛМП вони можуть замовити будь-яку комбінацію таких тестів:
- Загальний аналіз крові (CBC)
- Аспірація кісткового мозку
- Біопсія кісткового мозку
- Поперекова пункція
- Тести зображень (наприклад, рентген, КТ, МРТ)
- Цитогенетика
Цитогенетика та молекулярне тестування особливо важливі для визначення вашого підтипу. Це передбачає вивчення генетичного матеріалу вашої клітини під мікроскопом для виявлення генетичних відхилень, таких як транслокації та інверсії.
Діагностування лейкеміїПідтипи та лікування ПВК
Протягом останніх кількох років Управління з контролю за продуктами та лікарськими засобами схвалило безліч нових препаратів протидії відмиванню ліків; проте всі вони розроблялись задовго до того, як з’явилися дослідження 2016 року.
Зараз, в основному на основі цього дослідження, в даний час вивчаються численні потенційні методи лікування АМЛ на основі конкретних генетичних підтипів.
Кілька досліджуваних препаратів, які націлені на певні генетичні мутації, розпочали процес дослідження, і дослідники також розглядають нові типи хіміотерапевтичних препаратів, комбінації препаратів та антитіл та препарати, що називаються інгібіторами кінази.
Деякі з цих препаратів вже є на ринку за інших умов, тоді як інші показують багатообіцяючі результати у випробуваннях. Наприклад:
- Потенційні методи лікування мутації AML під назвою TET2 можуть включати препарати, які називаються інгібіторами PARP або HMA у поєднанні з вітаміном C.
- Група ферментів, що називається KAT, може допомогти лікувати AML з мутаціями в генах, що називаються EP300 та CBP.
- Лікарські засоби, що називаються активаторами p300, досліджуються на тваринних моделях AML.
Декілька інших генетичних підтипів AML досліджуються, щоб дослідники могли з'ясувати, які ліки можуть націлювати їх.
Варіанти лікування лейкеміїСлово з дуже добре
Гострий мієлоїдний лейкоз завжди був страшним діагнозом із поганим прогнозом.
Однак із появою нових ліків, які з’являються в дорозі, та постійними новими відкриттями про генетичні підтипи, прогноз покращується, і, ймовірно, буде продовжувати це робити.



















.jpg)