Басейн / Басейн / Getty Images
Ключові винос
- FDA надала дозвіл на екстрене використання вакцини COVID-19, розробленої Pfizer та BioNTech.
- Новини з’являються на наступний день після того, як консультативний комітет FDA рекомендував агентству дозволити вакцину
- Дані, розглянуті комітетом, визнали вакцину ефективною на 95%.
- Розповсюдження вакцин може відбутися протягом 24 годин після отримання дозволу.
У п'ятницю ввечері Адміністрація з харчових продуктів та медикаментів (FDA) надала дозвіл на екстрене використання своєї першої вакцини проти COVID-19. Вакцина, розроблена Pfizer Inc. та німецькою компанією BioNTech, розпочне розповсюдження найближчим часом.
Новини відбулися після довгоочікуваного публічного слухання в четвер, під час якого консультативна комісія FDA проголосувала 17-4 за підтримку дозволу на вакцину Pfizer, причому один утримався.
Pfizer представив дані клінічних випробувань, в яких брали участь 43 000 дорослих учасників. Раніше цього тижня FDA поділилася деякими з цих даних, включаючи той факт, що 95% людей у клінічному випробуванні, які отримували вакцину, не продовжували розвивати COVID -19. Побічні ефекти були незначними, включаючи озноб, слабкий біль та почервоніння в місці ін’єкції.
Дозвіл на екстрене використання (EUA) поширюється на людей віком від 16 років. Pfizer також проводить клінічні випробування щодо безпеки та ефективності вакцини у дітей віком до 12 років, і, як очікується, додасть також випробування для дітей молодшого віку.
Дані про безпеку та ефективність з інших груп населення все ще необхідні
Консультативна група FDA, яка називається Консультативний комітет з питань вакцин та супутніх біологічних продуктів (VRBPAC), рекомендує Pfizer вжити додаткових заходів, щоб забезпечити безпеку та ефективність вакцини для більшої кількості населення. Комісія радить збільшити кількість кольорових людей до постійних клінічних випробувань. Кольорові люди частіше, ніж білі люди, заражаються COVID-19 і помирають від вірусу.
Комісія також обговорила два зареєстровані випадки алергічних реакцій у людей, які отримали вакцину у Великобританії цього тижня, де вона вже була затверджена. Пол Оффіт, доктор медичних наук, директор навчального центру з вакцин у дитячій лікарні Філадельфії, запитав ведучих Pfizer про алергічні реакції, стурбовані тим, що люди з важкою алергією можуть не приймати вакцину. Офіт рекомендував також проводити дослідження вакцини у людей із поширеною алергією.
Великобританія рекомендує людям, які в анамнезі мали анафілаксію до ліків чи продуктів харчування, не отримувати вакцину. США можуть додати подібне попередження в тандемі з дозволу. Працівники FDA на засіданні повідомили колегії, що вони вже працюють над письмовою документацією для споживачів про безпеку та ефективність вакцини.
Що це означає для вас
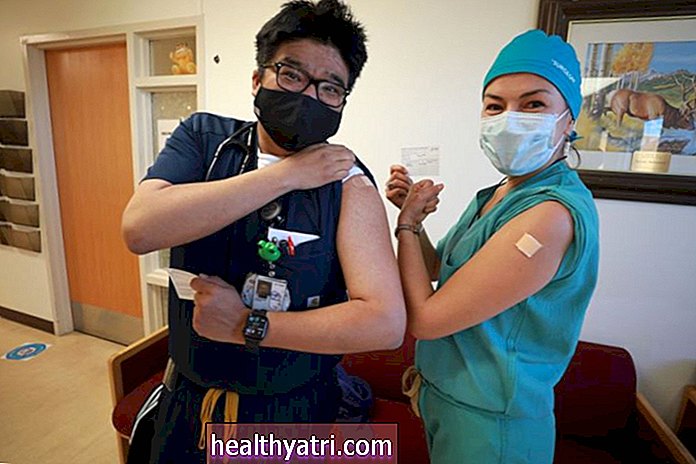
На підставі рекомендації дорадчого комітету дозволити вакцину Pfizer COVID-19, Управління з контролю за продуктами та ліками може затвердити її використання протягом декількох днів. Поширення може розпочатися дуже скоро після цього. Очікується, що перші дози вакцини будуть введені медичним працівникам та мешканцям будинків престарілих.
Після рішення VRBPAC, комісар FDA Стівен М. Хан, доктор медичних наук, опублікував заяву:
“Зазвичай процес перегляду вакцин, що вивчаються у десятків тисяч людей, займає місяці. Незважаючи на те, що процес був прискорений у зв'язку з переглядом цього EUA, експертний огляд FDA переглянув тисячі сторінок технічної інформації [включаючи] дані клінічних випробувань, неклінічні дані про розробку вакцини в лабораторії, та виробничі дані про те, як виготовляється вакцина ".
Хан, який, ймовірно, намагається вгамувати побоювання серед споживачів, додав: «У цей надзвичайний час співробітники FDA відчувають відповідальність за якнайшвидше просування процесу перегляду. Однак вони знають, що повинні виконувати свій мандат щодо захисту громадського здоров'я та забезпечення того, щоб будь-яка дозволена вакцина відповідала нашим суворим стандартам безпеки та ефективності, які очікували американці ».
Обраний президент Джо Байден також опублікував заяву після голосування в комітеті, сказавши: "Цілісність науки привела нас до цього".
FDA заявляє, що розподіл вакцин може відбутися протягом 24 годин після отримання дозволу.
Консультативний комітет FDA розгляне другу вакцину проти COVID-19, виготовлену Moderna, у четвер, 17 грудня.

-may-dampen-the-antibody-response-to-covid-19-vaccines.jpg)






.jpg)